|
|
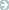 王玉杯理事長 致詞 王玉杯理事長 致詞 |
| |
|
|
|
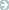 第一階段主持人:冼光祖副主委 第一階段主持人:冼光祖副主委
非新成分新藥委員會
晟德大藥廠(股)公司/處長 |
| |
|
|
|
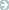 與會貴賓及講師 與會貴賓及講師 |
| |
|
|
|
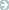 與會貴賓及講師 與會貴賓及講師 |
| |
|
|
|
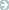 演講貴賓:呂瑞梅博士 演講貴賓:呂瑞梅博士
工研院生醫與醫材研究所
演講題目:由新劑型技術談產品加值策略 |
| |
|
|
|
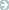 演講貴賓:陳本忠副主委 演講貴賓:陳本忠副主委
非新成分新藥委員會
南光化學製藥(股)公司/處長
演講題目:Rational Design of oral modified- release dosage
form |
| |
|
|
|
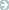 演講貴賓:顧曼芹主委 演講貴賓:顧曼芹主委
非新成分新藥委員會
展旺生命科技(股)公司/董事長
演講題目:Rational Design of injectable dosage form |
| |
|
|
|
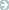 第二階段主持人:顧曼芹主委 第二階段主持人:顧曼芹主委
非新成分新藥委員會
展旺生命科技(股)公司/董事長 |
| |
|
|
|
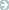 演講貴賓:孫懿真博士 演講貴賓:孫懿真博士
醫藥品查驗中心 藥劑科技組
演講題目:An Overview of CMC Postapproval Changes/
Variations from US FDA and EMA Perspectives |
| |
|
|
|
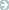 演講貴賓:鄒玫君研究員 演講貴賓:鄒玫君研究員
食品藥物管理署
演講題目:Global Regulation of complex products such as
liposome and nanoparticles. |
| |
|
|
|
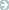 討論與交流:來賓提問 討論與交流:來賓提問 |
| |
|
|
|
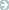 討論與交流:來賓提問 討論與交流:來賓提問 |
| |
|
|
|
 討論與交流:來賓提問 討論與交流:來賓提問 |
| |
|
|
|
 討論與交流:來賓提問 討論與交流:來賓提問 |
| |
|
|
|
 討論與交流 討論與交流 |
| |
|
|
|
 討論與交流 討論與交流 |
| |
|

















